【矩道化学虚拟实验室】质量守恒定律
更新时间:2022-08-17 来源:矩道科技 浏览:0
(人教版 九年级上册 第五单元 课题1 第1课时)
课程简介:
本文主要包括两部分内容:质量守恒定律和质量守恒定律的微观本质。通过复习旧知,提出发生化学反应时有新物质生成,即物质种类发生改变,自然引出疑问“反应前后物质的质量是否会发生改变”。对此进行实验探究,得到质量守恒定律。然后通过矩道化学仿真实验室观看水的电解实验微观动画,分析得出化学反应前后物质总质量不变的原因。
教学目标:
1.通过虚拟实验探究理解质量守恒定律,了解常见化学反应中的质量关系。
2.从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。
重点难点:
教学重点:
质量守恒定律的含义及应用。
教学难点:
1. 质量守恒定律的理解。
2.从微观角度认识在一切化学反应中,反应前后原子的种类和原子的数目没有增减。
教学流程设计
新课导入:
学生写出硫在氧气中燃烧,电解水反应的文字表达式,然后设置问题:化学反应特征是生成了新的物质,发生了质的变化,那么反应物的质量同生成物的质量之间具有什么样的关系呢?接下来让我们我们通过实验探究来找到答案。
环节一:质量守恒定律
1. 提出问题:
反应前后物质的质量之间具有什么关系?
2. 作出假设:
针对提出的问题,学生猜想、讨论,老师在学生发言后归纳出猜想:
① 反应后物质的总质量可能增加;
② 反应后物质的总质量可能减少;
③ 反应后物质的总质量可能不变;
④ 在某些反应中可能增加,在某些反应中可能减少,而在某些反应中可能不变。
3. 进行实验并记录数据:
学生利用矩道VR/3D融合创新实验室进行实验,并将实验现象记录在表格中:
① 红磷在密闭锥形瓶中燃烧。
② 铁与硫酸铜溶液反应。

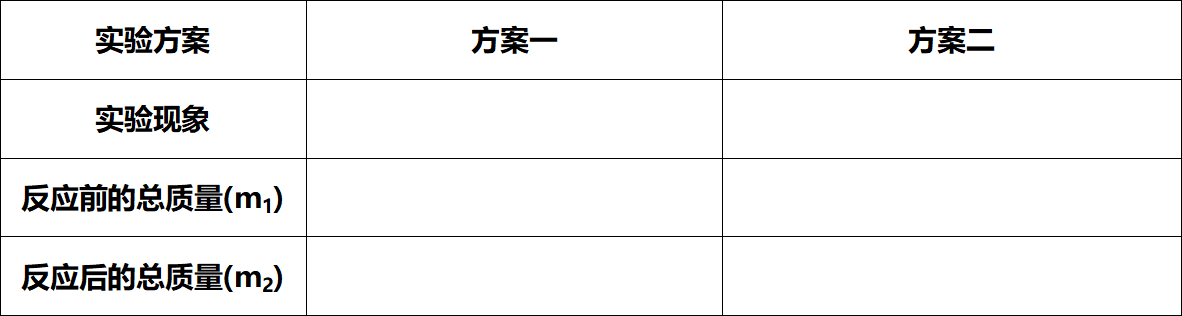
4. 分析并得出结论
实验完毕,各小组汇报结果,教师给予反馈,并归纳得出质量守恒定律:通过上述两个实验我们发现,发生化学反应时反应物的质量总和与生成物的质量总和存在相等的关系。实际上,不仅这两个实验如此,无数的实验证明,化学反应前后反应物和生成物的质量总和相等,这个规律叫做质量守恒定律。
5. 深化理解
教师:质量守恒定律是否对任何化学变化都适用呢?请同学们进行下面两个实验,观察反应前后天平指针的变化情况,并分析原因。
① 碳酸钠与稀盐酸反应
② 镁条在空气中燃烧


学生交流讨论,教师引导并总结:碳酸钠与盐酸反应因为有二氧化碳气体逸出反应体系,导致指针向右偏转;镁条实验,反应前称量的是镁条的质量,而镁条燃烧消耗了空气中的氧气,导致反应后增加了氧气的质量,指针向左偏转。质量守恒定律指参加化学反应的所有物质的总质量等于反应生成的所有物质的总质量,包括气体、液体和固体。
教师先提出问题:为什么在发生化学反应前后各物质的总质量相等?化学反应的微观实质是什么?然后展示电解水的微观动画,给学生必要的启迪。并提出以下拆分性的问题:
① 反应前后分子是否发生了改变?
② 反应前后原子是否发生了改变?(原子的种类、质量和数目)
③ 你能尝试从微观角度解释化学反应前后物质的质量关系吗?
学生独立思考后,进行小组讨论,然后进行组间交流得出反应前后各物质的质量总和相等的原因:原子的种类不变、原子的数目不变、原子的质量不变。
教师小结:从以上的讨论可以看出反应前后物质的质量之和之所以不变,是因为在化学变化中原子没有发生改变,包括原子的种类、质量和数目。
板书设计:
1. 质量守恒定律
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
2. 质量守恒定律的微观本质
化学反应的过程就是参加反应的各物质的原子重新组合而成其他物质的过程,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
总结:
本文主要包括两部分内容:质量守恒定律和质量守恒定律的微观本质。通过复习旧知,提出发生化学反应时有新物质生成,即物质种类发生改变,自然引出疑问“反应前后物质的质量是否会发生改变”。学生利用矩道VR/3D融合创新实验室进行实验,探究反应前后物质的质量关系,得出质量守恒定律。然后通过观看水的电解实验微观动画,分析得出化学反应前后物质总质量不变的原因:化学反应的过程就是参加反应的各物质的原子重新组合而成其他物质的过程,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
















