众所周知,在物质的一般分类中,酸和碱是两种重要的化合物。那什么是酸、碱呢?在Arrhenius酸碱理论中,在水中电离产生阳离子全部是氢离子的化合物叫做酸,阴离子全部是氢氧根的化合物就是碱。那问题产生了,水电离的时候既有氢离子,也有氢氧根,那水岂不既是酸又是碱? 或者,非水溶液中是不是就没有酸和碱了呢?
在历史中,人类对于酸碱的认知其实也是在不断改变的。
01
酸与碱
1923年,丹麦的物理化学家Johannes Nicolaus Brønsted和英国的Thomas Martin Lowry各自独立地提出了以他们名字命名的理论。在Brønsted-Lowry理论(下文通称酸碱质子理论)中,酸和碱是由它们相互反应的方式来定义的。

Johannes Nicolaus Brønsted(1879-1947)

Thomas Martin Lowry(1874-1936)
他们把酸定义为一种能提供质子的物质,比如氢离子,H+。他们将碱定义为能接受质子的物质,即质子受体。
02
共轭酸碱对(一)
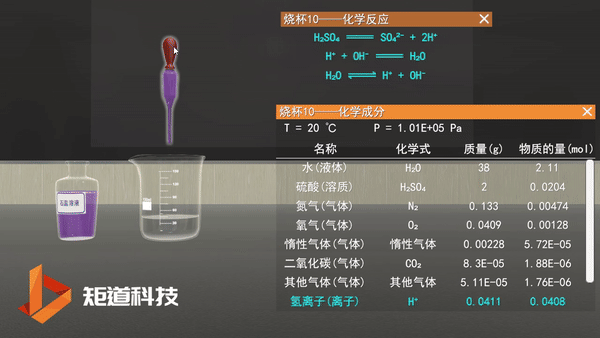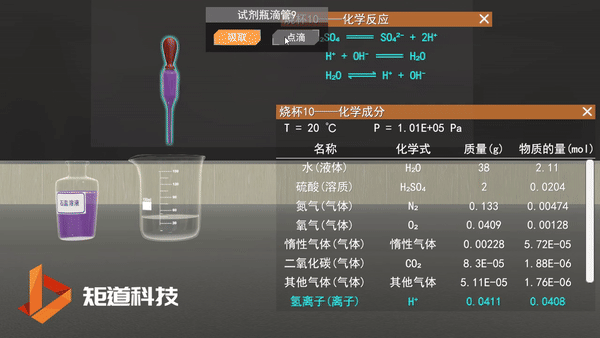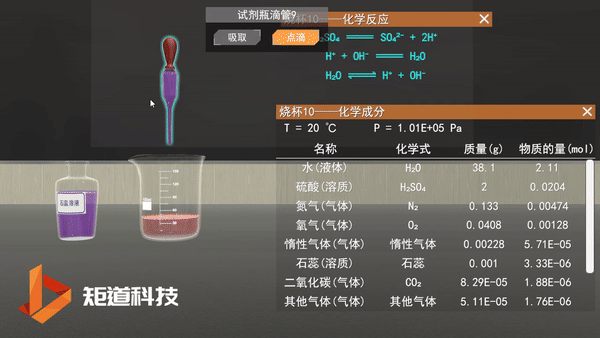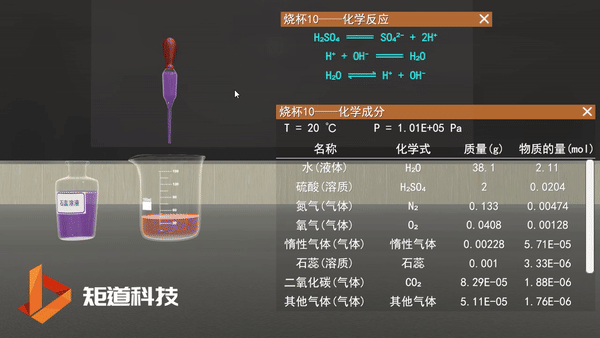
在过去,我们会认为稀盐酸里面会存在如图所示的电离:
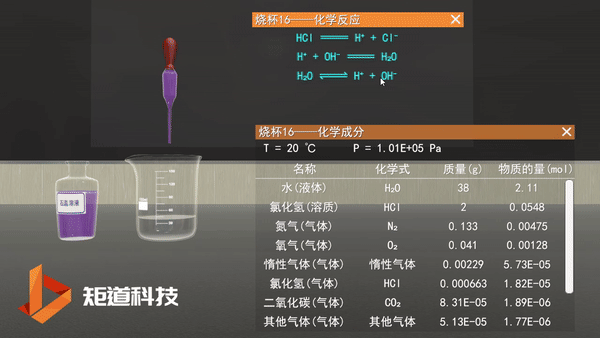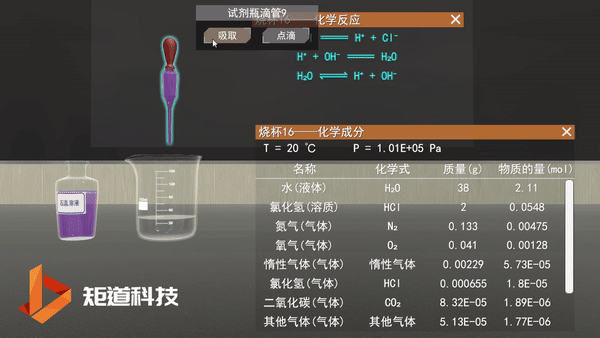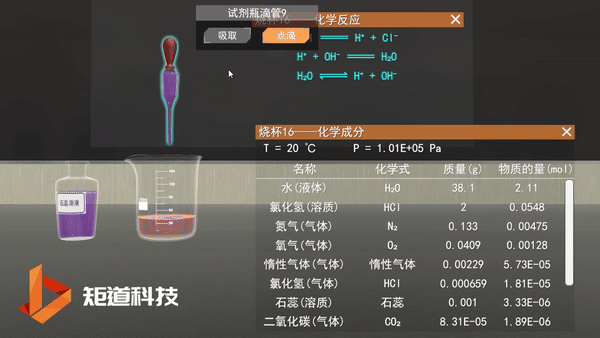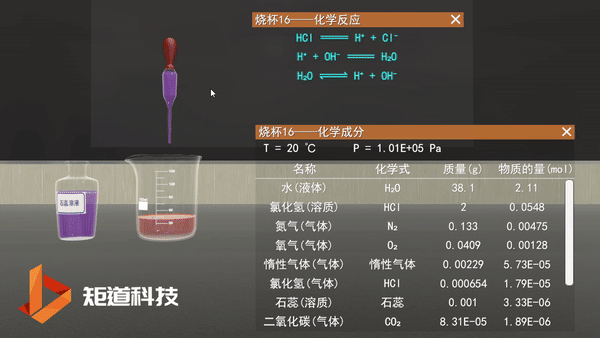
化学虚拟实验室——稀盐酸的电离
但在酸碱质子理论中,则认为会建立如下的平衡:
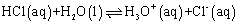
在正反应中:
·HCl表现为酸因为它给H2O提供了一个质子;
·H2O表现为碱因为它从HCI接受了一个质子。
在逆反应中:
·H3O+表现为酸因为它给Cl-提供了一个质子;
·Cl-表现为碱是因为它从H3O+接受了一个质子。
当酸HCI失去一个质子时,它形成碱Cl-。这两种物质称为共轭酸碱对。
当酸H3O+失去一个质子时,它形成碱H2O。这两种物质也形成共轭酸碱对。
因此上述平衡中包含两个共轭酸碱对:
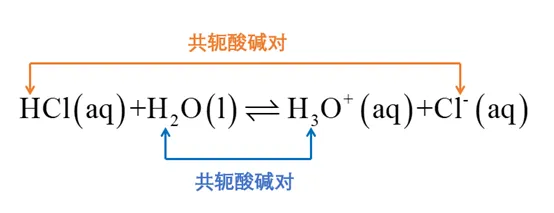
Cl-是HCl的共轭碱;H2O是H3O+的共轭碱。
盐酸可以提供一个质子,因此被称为一元酸。硫酸能提供两个质子,因此称为二元酸。
03
共轭酸碱对(二)
当氨溶于水时,平衡就建立起来了。

氨气溶于水的喷泉实验
下面的等式表示这种平衡:
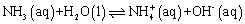
在正反应中:
·H2O表现为酸因为它给NH3提供了一个质子
·NH3表现为碱因为它从H2O接受了一个质子。
在逆反应中:
·NH4+表现为酸因为它给OH-提供了一个质子。
·OH-表现为碱是因为它从NH4+接受了一个质子。
所以这个平衡反应中同样存在两个共轭酸碱对:
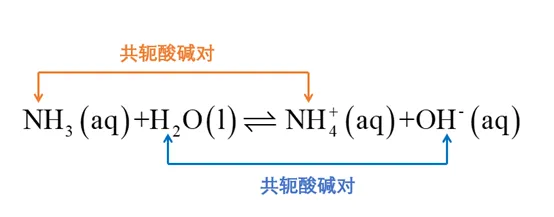
04
两性物质
在与HCI的反应中,H2O作为碱接受质子。然而,在它与NH3反应时,H2O通过提供质子而表现为酸。
像这种既能充当酸也能充当碱的物质被称为两性物质。
END
















