矩道化学虚拟现实课堂“物质结构与性质”模块,基于一线教学实践,以学科素养为指导,以开放性、探究性、学科性为主要目标,提供了原子、分子结构与性质、晶体结构与性质等丰富的VR数字课程资源超90个。

可自由操作互动性强,兼具常态化和新型教学互动,便于老师多样化教学,灵活掌控教学节奏。微观结构与原理可视化降低了教学内容抽象性,老师的教学不再停留在表面,可以更容易引导学生进行解释,促使学生反思原有概念模型的局限性,发展学生“证据推理与模型认知”等核心素养。

物质结构与性质模块,将抽象枯燥的微观粒子结构可视化,360度自由探究,形象生动;将晦涩难懂的结构组成规律原理可视化,情境过程化,直观明了;将抽象复杂的微粒性质与计算规律,思维模型外显化、规律情境化,助力高效教与学。每个内容提供了丰富的教学互动,在沉浸式的知识情境中可以灵活开展探究式学习,为教学评一体化背景下的高中化学沉浸式课堂提供了新助力、新方向、新思路!
配合物的价键理论不仅较好地说明了配合物的空间构型,也合理地阐明了配合物的许多性质。
01
配合物的稳定性
虽说配离子在溶液中都有较高的稳定性,但不同的配离子其稳定性大小是有差别的。例如 [FeF₆]³⁻和[Fe(CN)₆]³⁻,中心离子相同,且都是配位数为6的正八面体型配离子,而前者的稳定性不如后者。
Fe原子的核外电子排布,在失去三个电子后价电子为3d⁵
按价键理论的观点,这种差别正好与形成配离子的配位键型相关。[FeF₆]³⁻中的配位键为外轨配键,而[Fe(CN)₆]³⁻中的配位键为内轨配键。
类似的,[Ni(CN)₄]²⁻比[Ni(NH₃)₄]²⁺更稳定。
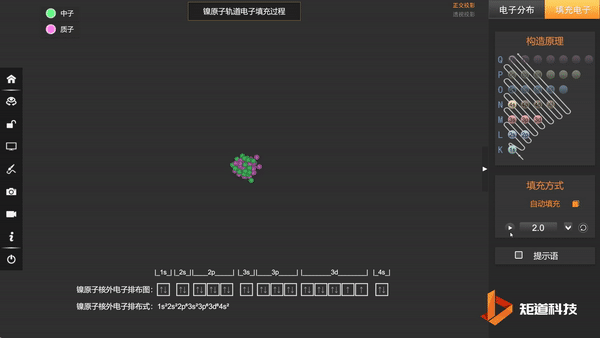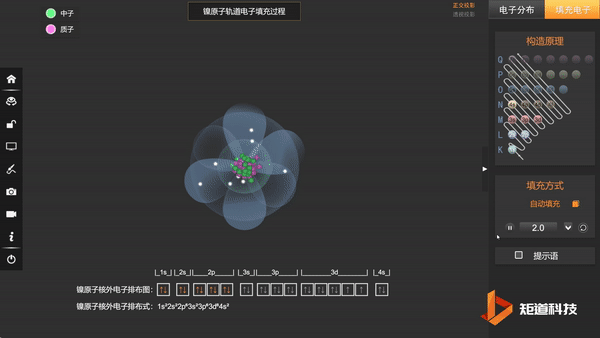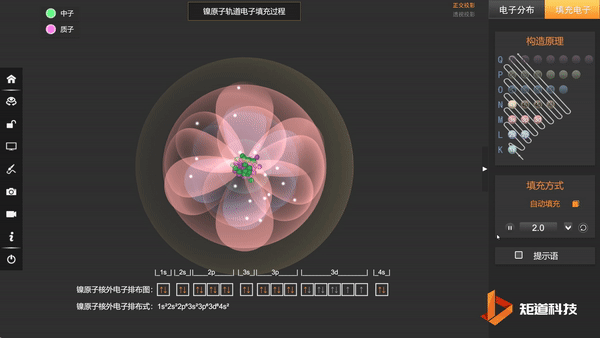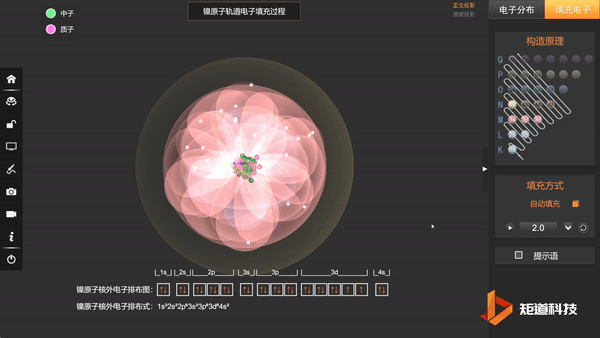
Ni原子的核外电子排布,失去两个电子后价电子为3d⁸
显然,内轨配键由于使用次外层(n-1) d轨道杂化成键,其能量低于次外层轨道的能量。由此可见,配位数相同的配子,一般内轨配合物要比外轨配合物稳定。
02
配合物的磁性
物质的磁性可用磁矩μ进行量度,μ的单位为玻尔磁子,用符号B.M.表示。通过实验测定配合物的磁矩,可了解配合物的磁性。例如,实验测得 K₃[FeF₆]、K₃[Fe(CN)₆]两种配合物的磁矩分别为 5.90 B.M.和2.0 B.M.。两种配合物磁性强弱明显不同。
究其原因,这是由于物质的磁性与物质中电子的自旋运动有关。若配离子结构中所有电子均已成对,正、逆方向自旋的电子所产生的磁效应刚好相互抵消,此时磁矩μ=0,磁矩为0的物质称为抗磁性物质。
反之,若配离子结构中存在未成对电子,则物质必表现为顺磁性,磁矩>0,而且磁矩的大小与未成对电子的数目有关。配合物磁性的测定是判断配合物结构的一个重要手段。
根据磁学理论,磁矩可用下式近似计算:
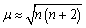
式中,n 是物质中未成对电子数。
比如,[FeF₆]³⁻的磁矩为5.90 B.M.,带入可得n约等于5,说明[FeF₆]³⁻中应有5个未成对电子,是外轨型配合物;[Fe(CN)₆]³⁻的磁矩为2.0 B.M.,可知其中应只有1个单电子,说明采取d²sp³杂化,3d轨道只有一个单电子。这与我们之前的理论结果相符合。由此可见,配合物的价键理论能较好地解释配合物的磁性。
END
















